当前,近红外二区(NIR-II,1000-1700nm)荧光成像已在生物医学基础研究和肿瘤术中精准切除等临床转化方面展现出巨大的应用前景。相较于近红外一区(NIR-I,700-1000 nm),近红外二区荧光成像所具备的在生物体内散射低、组织穿透深且成像分辨率高的优势,更使其被视为极具发展潜力的影像技术。
然而,受限于荧光成像的固有缺点,如较小的斯托克斯(Stokes)位移和较短的光学寿命,近红外二区荧光成像在动物活体内高分辨、高质量的实时成像效果仍不理想,依然有很大的空间予以提高。如何进一步从成像探针和成像方法方面对近红外二区成像进行重新思考与设计,是突破现有近红外二区成像生物应用瓶颈的关键。
近日,中科院自动化所胡振华研究员和武汉理工大学常柏松副研究员、中科院上海药物所程震教授、武汉理工大学孙涛垒教授合作,创新性地开发出了近红外二区磷光成像(NIR-II phosphorescent imaging)探针及技术,首次将磷光拓展到近红外二区区域,为探索面向重大疾病的特异性成像提供了新思路和新策略,为疾病的在体早期诊断、术中导航治疗提供了一种新的强有力的工具。相关工作(A phosphorescent probe for in vivo imaging in the near-infrared II window)发表于《自然》子刊Nature Biomedical Engineering杂志(https://www.nature.com/articles/s41551-021-00773-2)。
本研究通过金属离子交换机理,制备出具有空心结构的CuISe纳米管,利用氢键诱导的受限自组装原理,成功改变了纳米探针的受激态衰减过程,将近红外二区(最大发射峰在1130nm左右)磷光探针CuISe纳米管的荧光寿命从73ns延长到336μs。
基于CISe纳米探针的荧光-磷光转变机理,本研究还开展了小动物活体实时近红外二区磷光成像实验。实验结果表明,正常组织的背景噪声得到了明显抑制,近红外二区磷光成像具有显著的肿瘤特异性。尾静脉注射CISe纳米探针24h后,肿瘤的信噪比可达190,血管分辨率可达7.6μm,充分显示出近红外二区磷光成像具有在动物活体内高分辨、高质量实时成像的能力。
值得关注的是,近红外二区成像技术具有很高的临床转化潜力。此前,中科院分子影像重点实验室及其合作团队经过长期的研究积累和技术攻关,已在国际上首次(first-in-human)实现了近红外二区荧光成像的临床转化。实验结果表明,与传统成像技术相比,使用近红外二区荧光成像能够发现更多的肿瘤原发灶和转移灶。相关工作去年发表在Nature Biomedical Engineering杂志上(https://www.nature.com/articles/s41551-019-0494-0),同时得到了Nature Biomedical Engineering杂志专题评述及多位著名专家的高度评价。而此次,研究团队进一步把磷光拓展到近红外二区区域,可以实现肿瘤及血管更高分辨率、更高对比度、更大穿透深度的成像,在肿瘤更高特异性的早期精准诊断与术中荧光引导肿瘤精准切除等临床应用中看得更深、看得更清,对于继续推动近红外二区成像技术的临床转化工作具有重大意义。
相关研究工作得到了科技部国家重点研发计划“纳米科技”重点专项、国家自然科学基金委等项目的资助。
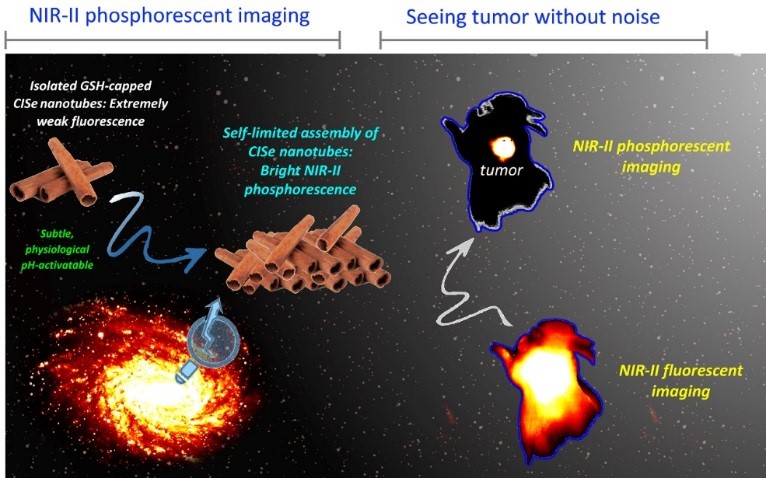
图1: CISe纳米管作为NIR-II磷光探针能够实现对肿瘤的高灵敏高特异性成像